УДК 543.862/.862.34
О. Тарасенко,
к.т.н., судовий експерт сектору дослідження наркотичних засобів, психотропних речовин, їх аналогів та прекурсорів відділу досліджень матеріалів, речовин та виробів,
Луганський НДЕКЦ МВС,
м. Рубіжне Луганської області
ORCID: https://orcid.org/0000-0001-9861-2256
тел.: +380994046302, email: Ця електронна адреса захищена від спам-ботів. вам потрібно увімкнути JavaScript, щоб побачити її.
Анотація: у статті висвітлено можливість кількісної ідентифікації 1-феніл-2-піролідин-1-іл-пентан-1-ону (далі - α-PVP) у складі сумішей для куріння (спайсів та вейпів), запропоновано методику визначення. Для реалізації поставленої мети вжито комплекс загальнонаукових і спеціальних методів. Систематизовано теоретичні матеріали з проблеми що вирішується; визначено стан практичної опрацьованості питання; організаційно-експериментальними засобами у поєднанні з якісним аналізом і математичною обробкою отриманих даних підтверджено ефективність запропонованої методики. Достовірність результатів забезпечено використанням сучасних інструментальних фізико-хімічних, математичних та статистичних методів аналізу. Визначено склад сумішей для куріння з використанням фізико-хімічних методів дослідження. Вперше проказана можливість кількісної ідентифікації α-PVP у складі вейпів та спайсів із застосуванням газової хроматографії у поєднанні з мас-спектрометрією. Перевірено ефективність відомих методів дослідження α-PVP і зроблено внесок у майбутнє формування методики з дослідження компоненту в складі нарковмісних сумішей для куріння. Запропоновано загальні підходи щодо вибору схеми дослідження α-PVP.
Ключові слова: α-PVP; якісний аналіз; суміші для куріння; вейпи; спайси; хромато-мас-спектроскопія; газорідинна хроматографія, гліцерин; пропіленгліколь.
Зміст наукової роботи.
Суміші для куріння часто містять нікотин і синтетичні психотропні речовини, обіг яких на території нашої країни обмежений. Наразі в Україні спостерігається стрімке підвищення попиту на курильні суміші типу спайсів (рослинної сировини, просоченої високоактивними хімічними реагентами), вейпів (рідких сумішей для куріння) тощо, які розповсюджують під виглядом ароматизаторів, прянощів та спецій через інтернет-магазини, різні служби доставки.
За короткий час через недосконалість законодавства вони стали доступні для роздрібної торгівлі приватними підприємствами, що різко позначилося на соціальній характеристиці контингенту споживачів [1].
Аналіз сумішей засвідчив, що основними їх компонентами є ароматизатори, нікотин, гліцерин і пропіленгліколь у різному співвідношенні. Рідина здебільшого складається з пропіленгліколю і гліцерину. Рослинна суміш – з носія, також просоченого рідким сорбентом. Є навіть спеціальні суміші для курців із непереносимістю того чи іншого інгредієнта. У їх складі зовсім немає пропіленгліколю чи гліцерину або їх мінімальна кількість. Суміші для куріння використовують, послуговуючись переважно так званими спайсами, вейпами айкосами тощо – спеціальними пристроями на кшталт звичайних електронних сигарет [2].
На перший погляд, зазначені основні компоненти особливої небезпеки не несуть. Проте дедалі частіше в сумішах для куріння, крім пропіленгліколю, гліцерину, з’являються заборонені засоби чи речовини. Наприклад, ɑ-РVР (1-феніл-2-піролідин-1-іл-пентан-1-он) або його синтетичні аналоги. Головний зиск із розповсюдження таких продуктів у тому, що додавання ɑ-PVP дуже вигідне для продавців, оскільки вартість цієї речовини на чорному ринку коштує всього копійки, а вистачить її на велику кількості дозованих одиниць.
Основна проблема полягає в тому, що достовірно ідентифікувати α-РVР чи його похідні у складі подібних сумішей вкрай важко через брак зразків для порівняння та даних про мас-спектри іонів у існуючих бібліотеках, зокрема в тих, що наявні у ДНДЕКЦ [3, 4].
Для вирішення цієї проблеми досліджено суміші для куріння невідомого складу та їх суміші з додаванням розчину ɑ-РVР, стандартні зразки якого наявні у Луганському НДЕКЦ.
Методика дослідження. З метою попереднього визначення ɑ-PVP у суміші проводився якісний хімічний аналіз. Брали краплину рідини (об’єкт 1). Для зручності та вивчення об’єктів у однакових умовах для твердої форми (об’єкт 2) проводили екстракцію етанолом: рослинну речовину із спайсу висушували, очищували розчином КОН, висушували та екстрагували етиловим 96%-вим спиртом (об’єкт 2). Отриманий екстракт упарювали за 70 ℃ до об’єму в кілька крапель. По краплі рідин (об’єкти 1, 2), що не містять та містять у складі PVP наносили на фільтрувальний папір, обприскували розчином роданіду кобальту та реактивом Манделіна.
Аналогічним чином робили підготовку об’єктів із додаванням до їх складу ɑ-PVP (до рослинної суміші та рідини за однакових умов додавали по 1,0 мл метанольного розчину ɑ-PVP з середньою концентрацією у 0,4777 мг/мл; суміш висушували, рідину гомогенізували).
У результаті в зразках об’єктів 1, 2 зміни кольору не відбулося. Натомість в зразках об’єктів 3, 4 спостерігали блакитне забарвлення, що свідчить про ймовірну наявність ɑ-PVP.
Дослідження методом тонкошарової хроматографії проводили з метою якісного визначення у складі суміші ɑ-PVP. По 5 мкл отриманих розчинів по краплі наносили на серію хроматографічних пластин «Sorbfil» ПТСХ-АФ-А-УФ (сорбент силікагель СТХ-1А; зерніння 10 мкм; товщина шару 110 мкм; єднальне силіказоль; індикатор УФ-254; тип підкладки Аl). Як зразок порівняння використовували стандартний метанольний розчин PVP.
Попереднє дослідження показало, що найефективнішими є дві системи розчинників:
І) гексан – хлороформ – ацетон (4:1:1); ІІ) гексан – ацетон (4:1). По закінченні процесу хроматографування пластини були висушені за температури 70 °С та далі візуально оглянуті при природному освітленні (за довжини хвилі λ = 550 нм) й в ультрафіолетових променях кварцової лампи (за довжини хвилі λ = 254 нм). Після огляду виявлені зони хроматографічних пластин були обприскані розчином роданіду кобальту та реактивом Манделіна. Після їх обприскування розчином роданіду кобальту відбулася характерна зміна кольорів.
У результаті на хроматографічних пластинах (табл. №1,2) утворилася серія зон.
Таблиця №1
Результати дослідження у системі «метанол – 25% розчин аміаку (100:1,5)»
|
Компонент |
Значення Rf |
Колір зони (обробка розчином нінгідрину в ацетоні) |
|
|
зразок порівняння |
екстракт об’єкта |
||
|
α-PVP |
0,70 |
0,70 |
оранжевий |
Таблиця №2
Результати дослідження у системі «циклогексан – толуол – діетиламін (75:70:10)»
|
Компонент |
Значення Rf |
Колір зони (обробка розчином роданіду кобальту) |
|
|
зразок порівняння |
екстракт об’єкта |
||
|
α-PVP |
0,81 |
0,81 |
блакитний |
Як відомо, основними чинниками, що впливають на якість ідентифікації складових суміші, є максимальний збіг кольору та розташування забарвлених зон на хроматографічних пластинках з аналогічними показниками у зразках порівняння, виготовлених зі стандартних речовин, а також ділянок поглинання при огляді в ультрафіолетовому випромінюванні [5, 6].
Таким чином, встановлено збіг Rf (хроматографічного коефіцієнта рухливості, що визначається як відношення відстані від лінії старту до центра зони об’єкта до значення відстані від лінії старту до лінії фронту розчинника) та кольору забарвлення хроматографічних зон об’єктів дослідження із розчинами зразків порівняння (метанольний розчин α-PVP).
Отже, екстракти об’єктів 3,4 дійсно містять α-PVP (1-феніл-2-піролідин-1-іл-пентан-1-он) – особливо небезпечну психотропну речовину, обіг якої заборонено.
Дослідження хромато-мас-спектрометричним методом. Для встановлення ɑ-PVP в об’єктах дослідження подальше якісне визначення проводили методом газової хроматографії з мас-селективним детектуванням [7].
Для цього до частини екстрактів додавали по 5 мл метанолу, перемішували. Розчини аналізували на хроматографі з мас-селективним детектором Shimadzu GCMS-QP2020 NX EI.
В результаті дослідження встановлено, що в об’єтах 3, 4 виявлений ɑ-PVP (мал. 1).
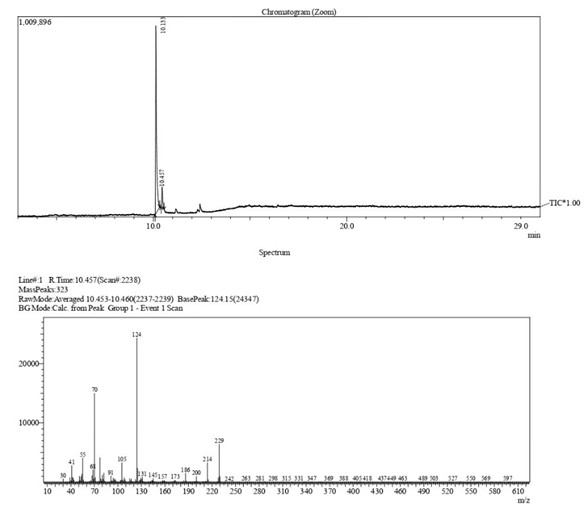
Мал. 1 GC-MS -спектр α-PVP у об’єктах 3, 4
З метою кількісного визначення α-PVP застосовували метод газової хроматографії.
До речовини об’єкта об’ємом 0,1 мл і до речовини (паралельний дослід) об’ємом 0,1 мл додавали по 5 мл суміші «хлороформ-діетиламін» (10:1). Після розшарування шари відокремлювали, екстракти об’єднували, аналізували на хроматографі Shimadzu GC-2010 Plus.
У результаті дослідження встановлено, що у складі об’єктів 3, 4 дійсно міститься α-PVP у концентрації 0,4562 мг/мл (мал. 2).
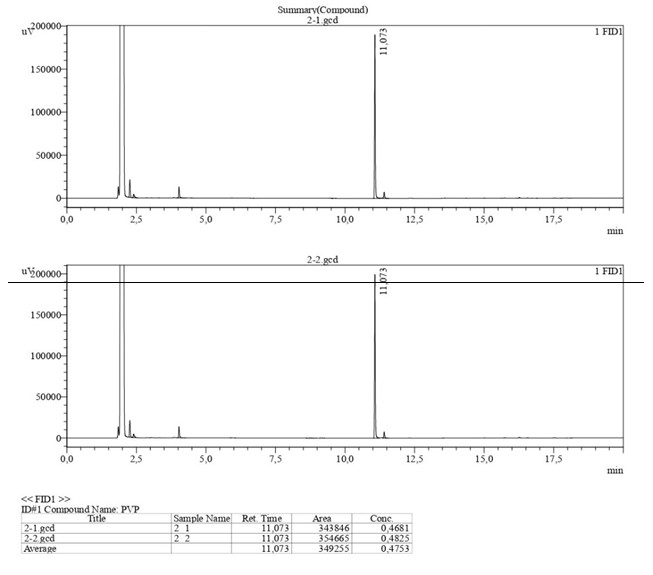
Мал. 2. Результати дослідження методом газової хроматографії
Для визначення концентрації α-PVP аліквоти отриманих екстрактів двічі аналізували на хроматографі програмою «LabSolution» методом абсолютного калібрування (табл. №3).
Таблиця №3
Результати газохроматографічного дослідження
|
Об’єкт |
Час утримання, хв |
Площа піка |
Концентрація, мг/мл |
|
3 |
11,073 |
343846 |
0,4681 |
|
4 |
11,073 |
354665 |
0,4825 |
Як видно з даних таблиці №3 значення концентрації ɑ-PVP у екстрактах об’єктів 3, 4 наближається до значення вихідної концентрації (табл. №4). Масу ɑ-PVP в об’єктах 3, 4 пропонується розраховувати за формулою:
|
Х = С•V/1000 |
- 1 |
де: С – концентрація ɑ-PVP за калібрувальним графіком, мг/мл;
V – об’єм екстрагента, мл.
Таблиця №4
Результати розрахунків селективності визначення ɑ-PVP
|
Номер об’єкта |
Концентрація поч., мг/мл |
Концентрація кін., мг/мл |
Селективність, % |
|
3 |
0,4715 |
0,4681 |
99,28 |
|
4 |
0,4839 |
0,4825 |
99,74 |
|
Сер. показники |
0,4777 |
0,4753 |
99,50 |
В результаті встановлена можливість кількісного визначення ɑ-PVP у складі сумішей для куріння із селективністю 99,5 % (незалежно від того тверда чи рідка форма суміші).
Висновки. Визначено склад сумішей для куріння типу спайс та вейп. Показана можливість кількісної ідентифікації в складі цих сумішей ɑ-РVР з використанням різних інструментальних методів (методом тонкошарової, газової хроматографії, мас-спектрометрії).
На конкретних прикладах перевірено ефективність чинної методики дослідження ɑ-РVР. Зроблено внесок у майбутнє складання методики з дослідження складу сумішей для куріння, що містять наркотичні та психотропні речовини.
Завдяки можливості ідентифікації у складі сумішей для куріння з’являється можливість швидкої діагностики наявності ɑ-PVP в організмі людини, а відтак – перспектива ефективної допомоги особам, які вживають суміші для куріння, на випадок їх передозування шкідливими складовими чи токсичного отруєння.
Література:
1. Балакірєва, О.М., Павлова, Д.М., Нгуєн, Н-М. К., Левцун, О.Г., Пивоварова, Н.П., Сакович, О.Т., & Флярковська, О.В. (2019). Куріння, вживання алкоголю та наркотичних речовин серед підлітків, які навчаються: поширення й тенденції в Україні: за результатами дослідження 2019 року в рамках міжнародного проекту «Європейське опитування учнів щодо вживання алкоголю та інших наркотичних речовин – ESPAD». Київ: Обнова компані. 214 с.
2. Кочеткова, С.К., Дурунча, Н.А., Пережогина, Т.А., & Остапченко, И.М. (2017). Исследование жидкостей для электронных систем доставки никотина. Международный научно-исследовательский журнал, 4 (58), ч. 4, 54–57.
DOI: 10.23670/IRJ.2017.58.103.
3. Kolesnikova, T.O., Khatsko, S.L., Demin, K.A., Shevyrin, V.A., & Kalueff, A.V. (2019). DARK Classics in Chemical Neuroscience: α-Pyrrolidinovalerophenone ("Flakka"). ACS chemical neuroscience, 10 (1), 168–174.
DOI: https://doi.org/10.1021/acschemneuro.8b00525.
4. Левченко, О.Е., Курділь, Н.В., & Луценко, О.Г. (2016). Феномен спайс: суміші для паління або нова хімічна зброя [The phenomenon of spice: smoking blends or a new chemical weapons]. Медицина невідкладних станів, 2 (73), 94–99. Взято з http://nbuv.gov.ua/UJRN/Medns_2016_2_12.
5. Логан, Баррі К. (13 вересня 2013). SOFT Designer Drug Committee Monographs: Alpha-PVP. Society of Forensic Toxicologists.
6. Sykutera M, Cychowska M, Bloch-Boguslawska E (Травень 2015). A Fatal Case of Pentedrone and α-Pyrrolidinovalerophenone Poisoning. Journal of Analytical Toxicology 39 (4): 324–9. PMID 25737339.
DOI: 10.1093/jat/bkv011.
7. Gannon BM, Galindo KI, Mesmin MP, Sulima A, Rice KC, Collins GT (Травень 2018). Relative reinforcing effects of second-generation synthetic cathinones: Acquisition of self-administration and fixed ratio dose-response curves in rats. Neuropharmacology 134 (Pt A): 28–35. PMC 5809320. PMID 28811192.
DOI: 10.1016/j.neuropharm.2017.08.018.

